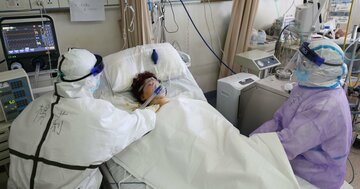
Photo:Reuters
Photo:Reuters
新型コロナウイルス感染症(COVID-19)の重症患者600人が、回復した患者の血漿(けっしょう)を投与する治療を受けている。この実験的治療は果たして患者の健康回復につながるのか、そして科学的厳密さを伴う伝統的臨床試験の枠外で有用なデータを生み出すのか。研究者らは、現在の取り組みがこうした疑問の答えとなることを期待している。
患者たちは、米食品医薬品局(FDA)が4月初めに承認した全米規模の拡大治療プログラムに参加している。(未承認薬の)例外的使用とも呼ばれる拡大治療は、承認された治療法のない致命的病気の患者や、臨床試験に参加できない患者のために人道的見地から行われることが多い。
例外的使用の研究で得られたデータの有用性は、医療・科学分野のコミュニティーでの議論の材料になることだ。この世界では、新薬の安全性と有効性に関する究極の判断基準は、はるか昔から比較臨床試験だった。こうした伝統的なランダム化(無作為に対象者をグループ分けした)試験では、1つのグループの患者が治験薬による治療を受け、比較対象となるもう1つのグループの患者は通常の治療を受けるか、またはプラシーボ(偽薬)を与えられる。
例外的使用を批判する人々は、同治療方法では研究に参加するすべての患者が同じ薬剤を与えられ、比較対象となる対照群(コントロールグループ)が存在しないため、薬効があったかどうかを知ることができないと指摘する。同治療の反対派はまた、実験的治療を受けられなくなるとの懸念から、伝統的臨床試験への参加に消極的になる患者が出てくることを懸念している。
コントロールグループが存在しなければ、研究者は何が治療効果の違いをもたらしたのか確実に判断することができない。年齢、性別、体重、基礎的健康条件、社会経済的地位、医師自身のバイアスなどのすべてが、患者の状態変化に影響する可能性がある。そして、COVID-19を含む多くの病気では、一部の患者は自力で回復する。このため、例外的使用はこれまで、信頼できるデータを提供するものではなく、患者に緊急措置として実験的治療を提供するものと受け止められてきた。
ミネソタ州ロチェスターのメイヨー・クリニックに勤務し、回復した患者の血漿による今回の拡大治療プロジェクトの調査責任者でもあるマイケル・ジョイナー氏は「拡大治療は、われわれに完璧なランダム化比較臨床試験と同じデータを提供するわけではない。だが、特殊な状況下で一定の知見を与えてくれる」と述べる。