Photo:CFoto/JIJI
Photo:CFoto/JIJI
小林製薬の紅麹成分を含んだサプリメントで健康被害が発生した問題を巡り、消費者庁の専門家検討会は5月23日、機能性表示食品の制度を見直す提言案を取りまとめた。内容は制度を厳格化するものだが、そこには深謀遠慮ものぞく。特集『薬局・薬剤師 サバイバルダンス』(全24回)の#13では、機能性表示食品制度見直しの動向を追った。(ダイヤモンド編集部副編集長 臼井真粧美)
品質管理や健康被害報告で
「義務なき」甘さ
小林製薬の紅麹成分を含んだサプリメントで健康被害が発生した問題は、機能性表示食品の安全性に“落とし穴”があることを露呈した。
機能性表示食品は2015年にスタートした制度の下、安全性や機能性の科学的根拠を事業者が消費者庁に届け出れば、事業者の責任において健康効果を表示できるものだ。
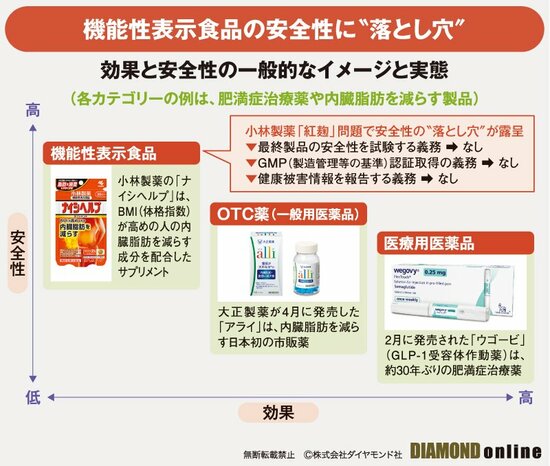
一般的なイメージでは、よく効くものほど安全性は低くなる。医師が処方する医療用医薬品は、処方箋なしで薬局で買えるOTC薬(一般用医薬品)よりも、OTC薬は機能性表示食品よりも、高い効果が期待できる。安全性については、その逆である(下図参照)。
ところが小林製薬事件では、機能性表示食品であるサプリが健康被害の問題を引き起こした。薬ではなく、食品であるにもかかわらずだ。
安全性に対するルールについて、医薬品は厳格に定められているのに対し、機能性表示食品は緩かったが故である。最終製品の安全性についての試験、品質を守るためのGMP(製造管理及び品質管理に関する基準)認証取得、健康被害情報の報告、これら医薬品で義務化されているものが、機能性表示食品では義務化されていなかった。
図では、各カテゴリーの例に肥満症の治療薬や内臓脂肪を減らす製品を挙げている。
医療用医薬品であるデンマークのノボ ノルディスクの肥満症治療薬「ウゴービ」はもちろんのこと、OTC薬である大正製薬の内臓脂肪減少薬「アライ」も、海外では医療用医薬品として長年使われてきた成分でありながら、日本で時間とカネをかけて有効性や安全性の試験を実施した。
対して、内臓脂肪を減らす成分を配合した小林製薬のサプリ「ナイシヘルプ」は、ナイシヘルプそのものではなく、成分についての文献や既存の情報を調査したにすぎない。
医薬品と機能性表示食品では、製品になるまでの開発工程も製品化した後のルールもまるで異なる。にもかかわらず、機能性表示食品は機能性を表示できるため、パッケージの表示や製品の形状ではその差が消費者には分かりにくかった。
安全性のルールがここまで異なることが消費者に露呈し、他社のサプリにまで買い控えが広がっている。消費者が機能性表示食品のサプリに戻ってくるかどうかは、今回の事件を機に、国がどのようにルールを見直すかが鍵を握る。
消費者庁が4月に緊急設置した専門家検討会は、5月23日に機能性表示食品の制度を見直す提言案を取りまとめた。